Il dolore, definito dall'Associazione Internazionale per lo Studio del Dolore (IASP) come "un’esperienza sensitiva ed emotiva spiacevole, associata ad un effettivo o potenziale danno tissutale o comunque descritta come tale", è un fenomeno intrinsecamente soggettivo. Lungi dall'essere una mera risposta sensoriale, esso coinvolge un complesso intreccio di elaborazione cognitiva e risposte comportamentali, influenzando profondamente la qualità della vita di un individuo. La cognizione, intesa come l'acquisizione, l'elaborazione, la conservazione e il recupero di informazioni, gioca un ruolo cruciale nella percezione del dolore, richiedendo valutazione, apprendimento, ricordo di esperienze passate e processo decisionale attivo.
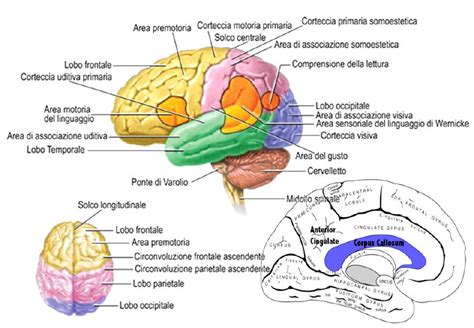
Le Reti Neurali del Dolore: Dalla Periferia al Centro
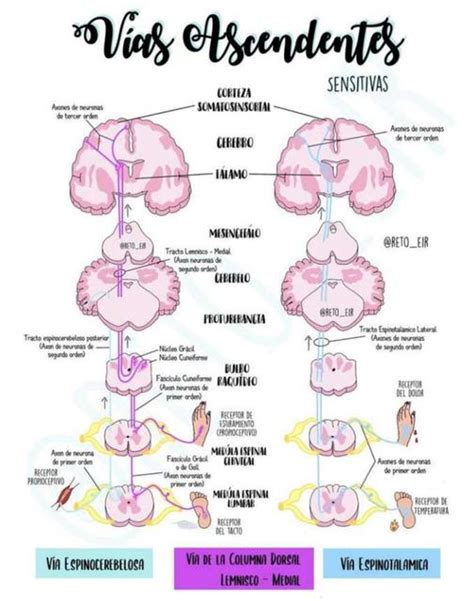
La trasduzione degli stimoli dolorosi inizia con i nocicettori specializzati, che convertono gli stimoli in segnali elettrici trasmessi attraverso le fibre nervose. Le fibre Aδ, responsabili della trasmissione di sensazioni tattili e termiche, e le fibre C, deputate alla trasmissione del dolore, proiettano ai gangli della radice dorsale (DRG). Qui, le fibre C modulano ulteriormente la sensibilità dei recettori NMDA, mentre a livello del midollo spinale, il rilascio di acido gamma-aminobutirrico contribuisce alla modulazione del segnale ascendente.
I tratti spinotalamici trasportano le sensazioni di dolore e temperatura lungo il midollo spinale ventrolaterale fino al talamo. Le proiezioni a formazioni reticolari, materia grigia periacqueduttale (PAG) e nuclei talamici mediali sono componenti fondamentali delle dimensioni motivazionali e affettive del dolore.
Un vasto circuito neurale corticale, comprendente i sistemi del dolore mediano e laterale, è coinvolto nella percezione, localizzazione e modulazione degli stimoli dolorosi. La via discendente del dolore coinvolge strutture sopraspinali come il midollo rostrale ventromediale (RVM), il tegmento pontomesencefalico dorsolaterale e il PAG. Nel sistema limbico, l'amigdala è intrinsecamente legata alla componente emotivo-affettiva del dolore e alla sua modulazione. Monoammine come serotonina (5-HT), dopamina (DA) e noradrenalina (NE) sono cruciali per la modulazione della via discendente, agendo prevalentemente sulle lamine I e II del midollo spinale.
Neuroplasticità e Dolore Cronico: Un Cervello in Trasformazione
La neuroplasticità, ovvero la capacità del cervello di modificare la propria struttura e funzione in risposta a stimoli ambientali, apprendimento e memoria, è un processo fondamentale per l'adattamento. Nel contesto del dolore, la neuroplasticità si riferisce ai cambiamenti che alterano la risposta dell'individuo al dolore, portando allo sviluppo di dolore cronico o ipersensibilità. Studi di imaging hanno rivelato una riorganizzazione spazio-temporale dell'attività cerebrale nel dolore cronico, con uno spostamento progressivo della rappresentazione del dolore dalle strutture sensoriali a quelle emotive e limbiche.
La corteccia prefrontale mediale (mPFC) sembra giocare un ruolo chiave nell'interazione cortico-limbica, modulando la risposta dell'amigdala. Questa interazione apre potenziali vie per nuove tecniche di controllo del dolore, incentrate sulla modulazione dell'amigdala da parte della mPFC. Le differenze interindividuali nella gestione degli stimoli nocivi e il livello di ansia influenzano questa plasticità. Fattori neurotrofici, lipidi neuro-modulatori e neuropeptidi, come il BDNF (fattore neurotrofico derivato dal cervello), sono implicati nello sviluppo della plasticità sinaptica e della neurogenesi nei circuiti del dolore.
Un esempio classico di neuroplasticità nel dolore cronico è il dolore neuropatico da arto fantasma. Stimoli nocivi ripetitivi possono indurre cambiamenti disadattivi nel SNC, manifestandosi come iperalgesia (percezione esagerata di stimoli lievemente dolorosi) o allodinia (percezione di dolore da stimoli normalmente non dolorosi). L'attivazione spontanea dei DRG può contribuire al fenomeno del "wind-up", un aumento progressivo dell'attività neuronale in risposta a stimoli ripetitivi. Quando gli stimoli sensoriali agiscono su meccanismi neurali centrali modificati, l'output è influenzato dalla memoria di esperienze dolorose passate.
L'Impatto del Dolore Cronico sulle Funzioni Cognitive
Il dolore cronico, definito come dolore che persiste per più di 3 mesi, trascende la sua origine e ha effetti deleteri sugli aspetti psicosociali dell'individuo, compromettendo la qualità della vita e i domini funzionali. La relazione tra dolore e cognizione è bidirezionale: il dolore può alterare le funzioni cognitive e, viceversa, le alterazioni cognitive possono influenzare la percezione e la gestione del dolore.
Attenzione: Un Faro Spesso Offuscato dal Dolore
L'attenzione, la capacità di focalizzare l'elaborazione delle informazioni, è una funzione globale che coinvolge strutture corticali e sottocorticali. Esiste una sovrapposizione tra le vie del dolore e la matrice attentiva, rendendo lo studio dell'attenzione nel contesto del dolore particolarmente significativo. Nei giovani adulti e negli adulti di mezza età, compiti cognitivamente impegnativi possono aiutare a deviare l'attenzione e autogestire il dolore. Tuttavia, negli anziani, questa capacità è limitata, e il dolore cronico può compromettere l'indipendenza, aumentando il rischio di disabilità fisica, ricovero e mortalità. Comorbilità come depressione e ansia possono ulteriormente impattare negativamente sia sulla percezione del dolore che sull'attenzione. Studi clinici hanno evidenziato una maggiore incidenza di deficit attentivi in pazienti con dolore cronico, con particolare riferimento a difficoltà nella commutazione dell'attenzione e nell'attenzione divisa, come osservato in pazienti con fibromialgia.
Cos'è il dolore cronico?
Memoria: Ricordi Alterati da Sofferenze Prolungate
La memoria, essenziale per l'apprendimento e la cognizione, comprende sistemi di immagazzinamento a breve e lungo termine, con la memoria di lavoro che gioca un ruolo chiave nel controllo del flusso informativo. Il dolore cronico è associato a una riduzione del volume dell'ippocampo e della plasticità strutturale e biochimica. Anche l'amigdala, cruciale per l'apprendimento, è influenzata, con l'attivazione basolaterale in presenza di glucocorticoidi che impatta sul consolidamento della memoria. Le prestazioni e il recupero della memoria di lavoro sono compromessi in presenza di elevati livelli di glucocorticoidi. Studi hanno dimostrato un impatto negativo del dolore cronico sulla memoria di lavoro, sul ricordo e sulla memoria di riconoscimento, mentre la memoria implicita (semantica, procedurale, condizionata) tende ad essere meno influenzata. L'apprendimento spaziale, il riconoscimento e la memoria sono compromessi in presenza di dolore cronico, con una minore accuratezza e un aumento della latenza di risposta in compiti cognitivamente impegnativi.
Funzioni Esecutive: Pianificazione e Controllo Sotto Assedio
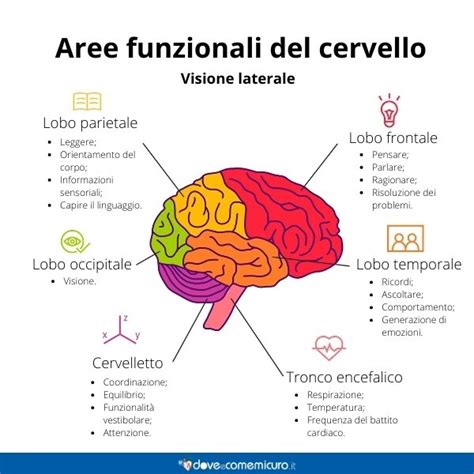
Le funzioni esecutive, regolate dai lobi frontali, comprendono processi cognitivi complessi come pianificazione, organizzazione, controllo dei pensieri e autoregolazione. Esiste una sovrapposizione funzionale tra le vie cerebrali deputate alle funzioni esecutive e quelle coinvolte nella percezione del dolore. Nei pazienti con dolore cronico, si osserva una diminuzione del volume in aree come l'ACC (corteccia cingolata anteriore), l'insula (IC) e la corteccia prefrontale dorsolaterale (DLPC). Sebbene alcuni studi non abbiano evidenziato impatti significativi sulla cognizione complessiva, la tipologia di dolore cronico sembra definire l'impatto sulle funzioni esecutive. Ad esempio, il processo decisionale emotivo è maggiormente compromesso nei pazienti con lombalgia cronica rispetto a quelli con sindrome dolorosa regionale complessa (CRPS). L'intensità e la natura della sindrome da dolore cronico possono influenzare la velocità di elaborazione e i compiti di interferenza attentiva, mentre il numero di siti dolorosi e la durata della neuropatia correlano positivamente con l'efficienza psicomotoria.
Gestione del Dolore e Impatto Farmacologico
La gestione del dolore cronico rappresenta una sfida clinica significativa. Le modalità di controllo del dolore comuni si concentrano sulla componente sensoriale, spesso avvalendosi di farmaci antinfiammatori non steroidei (FANS) e oppioidi. I recettori oppioidi sono presenti in aree neurali associate alla segnalazione e percezione del dolore. Gli oppioidi agiscono su PAG, RV e midollo spinale per modulare la percezione degli input nocicettivi. Tuttavia, il loro uso è associato a effetti collaterali come stipsi, sedazione, nausea e prurito. Nonostante ciò, gli oppioidi rimangono tra gli analgesici più prescritti per il dolore cronico, data la loro efficacia.
Un consumo elevato di oppioidi può però compromettere specifici domini cognitivi, in particolare attenzione, linguaggio, orientamento e funzione psicomotoria. Il follow-up periodico è essenziale per diagnosticare precocemente eventuali cambiamenti cognitivi lievi. Evidenze suggeriscono che i bambini esposti a oppioidi in utero tendono a mostrare una maggiore incidenza di disfunzione cognitiva e problemi attentivi. Studi recenti indicano una diminuzione volumetrica della materia grigia e una ridotta modulazione bilaterale dell'amigdala in seguito a somministrazione prolungata di morfina.
L'interesse per gli analgesici preventivi in ambito chirurgico è in crescita, così come la ricerca sugli endocannabinoidi (EC) come potenziale target terapeutico per il controllo del dolore.
Dolore e Disturbi Cognitivi: Una Sfida Assistenziale
Il sintomo dolore è spesso difficile da riconoscere in soggetti affetti da disturbi cognitivi, rappresentando un problema significativo in diversi contesti assistenziali. L'incapacità di comunicare verbalmente rende fondamentale l'uso di scale di valutazione specifiche per garantire che il dolore venga riconosciuto, registrato e trattato.
Nei soggetti con decadimento cognitivo, la difficoltà nel riconoscere, ricordare, quantificare e comunicare spontaneamente il dolore porta a una maggiore probabilità di sottotrattamento. Il dolore viene espresso attraverso segnali comportamentali, alterazioni neurovegetative, disturbi del sonno e dell'appetito, disturbi motori e vocalizzazioni.
La Scala PAINAD (Pain Assessment in Advanced Dementia) è emersa come uno strumento particolarmente indicato per rilevare il dolore in pazienti con demenza, grazie alla sua rapidità di somministrazione e adattabilità a diversi setting. Altre scale osservazionali validate in italiano includono la Abbey Pain Scale (ABBEY), la Non-Communicative Patient’s Pain Assessment Instrument (NOPPAIN), la Discomfort Scale-Dementia of Alzheimer Type (DS-DAT) e la ALGOPLUS.
È fondamentale una formazione adeguata per gli infermieri e gli operatori sanitari sulla valutazione e gestione del dolore, specialmente in pazienti che non utilizzano la comunicazione verbale. La creazione di team multidisciplinari con una solida base guida è essenziale per fornire un'assistenza efficace.
La complessità della valutazione del dolore in popolazioni con disturbi cognitivi evidenzia la necessità di strumenti validati e culturalmente adattati, considerando la scarsità di studi condotti su popolazioni non occidentali.
Classificazione del Dolore: Oltre la Semplice Sensazione
La classificazione del dolore è essenziale per orientare le decisioni cliniche e terapeutiche. Il dolore può essere classificato in base al meccanismo (nocicettivo, neuropatico, nociplastico), al tempo (acuto, ricorrente, persistente) e alla qualità/comportamento.
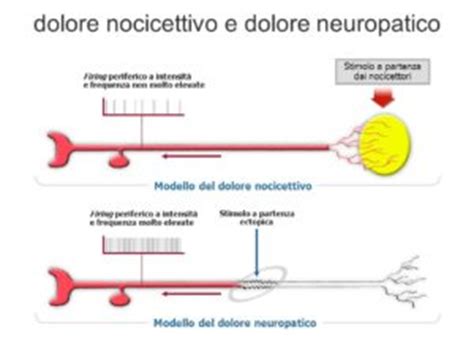
- Dolore Nocicettivo: Legato a stimoli provenienti dai tessuti (muscoli, articolazioni, visceri). Tende a modificarsi con il movimento e spesso coerente con una fase di irritazione o guarigione tissutale.
- Dolore Neuropatico: Deriva da lesioni o disfunzioni del sistema nervoso somatosensoriale. Si manifesta con bruciore, scosse, formicolio, intorpidimento o risposte dolorose sproporzionate.
- Dolore Nociplastico: Legato a un'alterazione della nocicezione senza chiara evidenza di danno tissutale o lesione nervosa. Il sistema diventa più sensibile e reattivo.
Queste componenti possono coesistere e variare nel tempo. Il dolore acuto indica un evento recente o una fase di allarme, mentre il dolore persistente (spesso definito cronico) indica una durata prolungata che può influenzare le scelte quotidiane e il modo in cui il sistema nervoso reagisce.
Fattori Contestuali e la Componente Cognitiva
Lo stress, le preoccupazioni, le esperienze passate, le aspettative e il contesto sociale influenzano profondamente l'interpretazione degli stimoli da parte del sistema nervoso. In situazioni percepite come pericolose, il sistema entra in allerta, amplificando i segnali dolorosi. Questo meccanismo, protettivo nel breve termine, può contribuire alla persistenza del dolore se mantenuto nel tempo. La componente cognitiva, inclusa la tendenza a catastrofizzare, gioca un ruolo centrale nella paura associata alle esperienze dolorifiche.
La terapia cognitivo-comportamentale (CBT) per il dolore cronico si focalizza sul cambiamento della risposta e della relazione con il dolore, modificando pensieri, credenze, emozioni e comportamenti che influenzano l'esperienza dolorosa. Tecniche come il rilassamento e la mindfulness sono strumenti potenti per ridurre la percezione del dolore. L'accettazione, come promossa dalla Acceptance and Commitment Therapy (ACT), implica l'esposizione al dolore senza tentativi di evitarlo o controllarlo, mentre si persistono in attività salutari.
È fondamentale riconoscere la realtà del dolore sperimentato dal paziente, sia a livello fisico che mentale, e affrontare le comorbilità psichiatriche come depressione e ansia, che possono esacerbare o causare dolore.
Conclusioni sull'Approccio Multidimensionale al Dolore
Il dolore è un'esperienza complessa e multidimensionale che va ben oltre la mera sensazione fisica. La sua percezione è intrinsecamente legata a fattori cognitivi, emotivi e comportamentali, mediati da intricate reti neurali. La comprensione delle diverse componenti del dolore, dalla sua origine nocicettiva o neuropatica alla sua alterata elaborazione nociplastica, è cruciale per un'efficace gestione.
Il dolore cronico, in particolare, impone un tributo significativo alla qualità della vita, compromettendo le funzioni cognitive, l'attenzione, la memoria e le funzioni esecutive. La neuroplasticità gioca un ruolo ambivalente, contribuendo sia alla cronicizzazione del dolore che offrendo potenziali vie per la riabilitazione.
La gestione del dolore richiede un approccio olistico che integri interventi farmacologici, terapie psicologiche come la CBT e l'ACT, e un'attenta valutazione delle componenti cognitive ed emotive. Per i pazienti con disturbi cognitivi, l'uso di scale di valutazione osservazionali e la formazione degli operatori sanitari sono indispensabili per garantire un'assistenza adeguata. In definitiva, riconoscere il dolore come un'esperienza soggettiva e complessa, influenzata da una miriade di fattori, è il primo passo verso un trattamento efficace e un miglioramento della qualità della vita.
tags: #tre #tipi #di #componenti #del #dolore
